lunes, 10 de septiembre de 2018
semana#30
Cuarto periodo
Proyectos de emprendimiento
- Proyecto newton - Quien quiere ser millonario}
- Bio qca- m.o - Aperitivos
Proyectos escogido
Productos lácteos
Títulos
Objetivos
Materiales
Marco teórico
Presentación del producto
Muestra
Productos que se haran
Yogurt
Kumis
Cuajada
Araquipe
Panelitas de coco
Integrantes
Manuela Murillo
Susna Gracia Loaiza
Any Guzman
Sonia Contreras
William Perez Marrugo
Proyectos de emprendimiento
- Proyecto newton - Quien quiere ser millonario}
- Bio qca- m.o - Aperitivos
Proyectos escogido
Productos lácteos
Títulos
Objetivos
Materiales
Marco teórico
Presentación del producto
Muestra
Productos que se haran
Yogurt
Kumis
Cuajada
Araquipe
Panelitas de coco
Integrantes
Manuela Murillo
Susna Gracia Loaiza
Any Guzman
Sonia Contreras
William Perez Marrugo
domingo, 2 de septiembre de 2018
semana#28
Mecanismo de las reacciones orgánicas
Ruptura y/o formación de enlaces
Toda reacción química implica una ruptura de los enlaces existentes en las moléculas que reaccionan y la formación de otros nuevos en los productos resultantes. El estudio de los mecanismos de las reacciones, nos lleva a considerar la serie de pasos concretos que se producen en la transformación de las sustancias reaccionantes en productos de reacción.
Teniendo en cuenta el mecanismo de ruptura o formacion de enlaces, las reacciones se clasifican:
a) Reacciones de homólisis / homogénicas
b) Reacciones de heterólisis / heterogénicas
c) Reacciones pericíclicas
semana#27
REACCIONES ORGANICAS
*Los enlaces son fuertes, normalmente las energías de activación son elevadas y las velocidades de reacción lentas
* Para acelerarlas es habitual o bien el uso de catalizadores, o la elevación de la temperatura
i) Según la forma de ruptura o formación de enlaces:
*Reacciones homolíticas (homo-lisis = igual-ruptura): Estas reacciones involucran radicales.
*Reacciones heterolíticas (hetero-lisis = diferente-ruptura): Estas reacciones involucran iones: carboaniones y carbocationes
ii) Según la relación existente entre los reactivos y los productos de la
reacción:
* Reacciones de adición:
Son aquellas en las cuales todos los átomos de los reactivos van a formar parte
de un único producto. Uno de los reactivos (al que podemos llamar sustrato)
debe contener un enlace doble, o uno triple:
*Reacciones de eliminación:
Son conceptualmente opuestas a las de adición. En este tipo de reacciones, a
partir de un compuesto y generalmente por acción de un segundo reactivo, se
produce la pérdida de los átomos equivalentes a una molécula pequeña, y la
formación de un nuevo producto, insaturado (con enlace doble o triple):
*Reacciones de sustitución:
Son las que involucran dos reactivos de los cuales uno es el sustrato, y el otro
es una molécula o ión generalmente pequeño (el que sustituye); los cuales
forman otra molécula y otra entidad pequeña (molécula o ión) (la cual es
desplazada).
semana#26
LABORATORIO:

REACCIONES ORGÁNICAS
Proposito:
-Reconocer experimentalmente aldehídos y cetonas, acidos carboxílicos y obtener acetileno.
-Reconocer las propiedades fisicas de algunos compuestos.
Proposito:
-Reconocer experimentalmente aldehídos y cetonas, acidos carboxílicos y obtener acetileno.
-Reconocer las propiedades fisicas de algunos compuestos.

semana#25
Isomería Óptica
semana#24
Enantiomeros y diastereómeros
El diastereomerismo se produce cuando dos o más estereoisómeros de un compuesto tienen configuraciones diferentes en una o más, pero no todas las equivalentes relacionadas. Los estereocentros no son imágenes especulares uno del otro. Cuando dos diastereoisómeros se diferencian entre sí en un solo estereocentro, son epímeros. Cada estereocentro da lugar a dos configuraciones diferentes y por lo tanto aumenta el número de estereoisómeros en un factor de dos.
Los diastereoisómeros se diferencian de los enantiómeros ya que estos últimos son los pares de estereoisómeros que difieren de todos los estereocentros y por lo tanto son reflejos uno del otro. Los enantiómeros de un compuesto con más de un estereocentro también son llamados diastereoisómeros de los otros estereoisómeros del compuesto que no es su imagen especular. Los diastereómeros tienen diferentes propiedades físicas y diferente reactividad, a diferencia de los enantiómeros.
semana#23
Isomeria conformacional
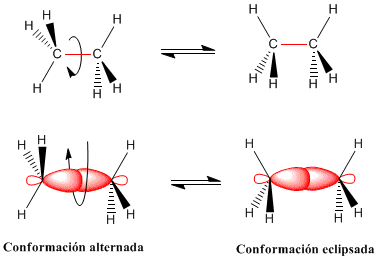
los enlaces simples entre átomos tienen simetría cilíndrica y permiten la rotación de los grupos que unen. Las diferentes disposiciones espaciales que adoptan los átomos como consecuencia de la rotación en torno al enlace se llaman conformaciones. Una conformación concreta de las múltiples posibles se denomina confórmero.
La rotación del enlace carbono-carbono en el etano da lugar a dos conformaciones límite -la conformaciones alternada (con los hidrógenos alternados) y la conformación eclipsada (con los hidrógenos enfrentados-. El paso de la conformación alternada a la eclipsada o viceversa se realiza por giro de 60º. Obsérvese que en un giro de 360º existen infinitas conformaciones posibles.
semana#22
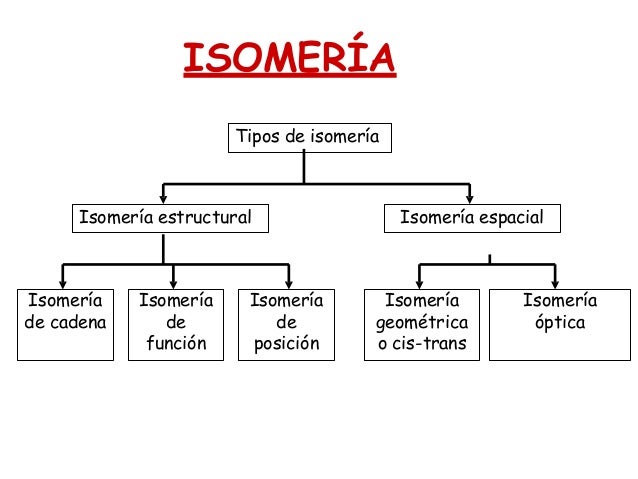
Isomeria estructural
existen 3 tipos:
*ISOMEROS DE CADENA:
Los isómeros de este tipo tienen componentes de la cadena acomodados en diferentes lugares, es decir las cadenas carbonadas son diferentes, presentan distinto esqueleto o estructura.
Un ejemplo es el pentano, del cual existen varios isómeros, pero los más conocidos son el isopentano y el neopentano.
Es la de aquellos compuestos en los que sus grupos funcionales están unidos en diferentes posiciones.
Un ejemplo simple de este tipo de isomería es la del pentanol, donde existen tres isómeros de posición: 1-pentanol, 2-pentanol y 3-pentanol.
*ISOMERIA DE FUNCIÓN:
Aquí, la diferente conectividad de los átomos, puede generar diferentes grupos funcionales en la cadena. Un ejemplo es el ciclohexano y el 1-hexeno, que tienen la misma fórmula molecular (C6H12), pero el ciclohexano es un alcano cíclico o cicloalcano y el 1-hexeno es un alqueno.
ISOMERIA ESPACIAL
Se clasifican en 2:
*GEOMETRICA CIS-TRANS:
La isometría cis-trans es un tipo de estereoisomería, la cual se refiere a los compuestos que tienen sus átomos conectados en el mismo orden pero tienen diferente orientación tridimensional. Este tipo de isomería presenta en cicloalcanos (serie de carbonos que conforman un anillo) y en alquenos (cadena de carbonos unidos por una doble ligadura). Se produce cuando existen dos grupos idénticos para comparar y se encuentran en diferentes posiciones.
* ISOMERIA OPTICA:
Cuando un compuesto tiene al menos un átomo de Carbono asimétrico o quiral, es decir, un átomo de carbono con cuatro sustituyentes diferentes, pueden formarse dos variedades distintas llamadas estereoisómeros ópticos, enantiómeros, formas enantiomórficas o formas quirales, aunque todos los átomos están en la misma posición y enlazados de igual manera. Esto se conoce como regla de Le Bel-van't Hoff

semana#21
Isomeria
La isomería es una propiedad de ciertos compuestos químicos que con igual fórmula química, es decir, iguales proporciones relativas de los átomos que conforman su molécula, presentan estructuras moleculares distintas y, por ello, diferentes propiedades. Dichos compuestos reciben la denominación de isómeros. Los isómeros son compuestos que tienen la misma fórmula molecular pero diferente fórmula estructural y, por tanto, diferentes propiedades. Por ejemplo, el alcohol etílico o etanol y el éter dimetílico son isómeros cuya fórmula molecular es C2H6O.

Suscribirse a:
Comentarios (Atom)





