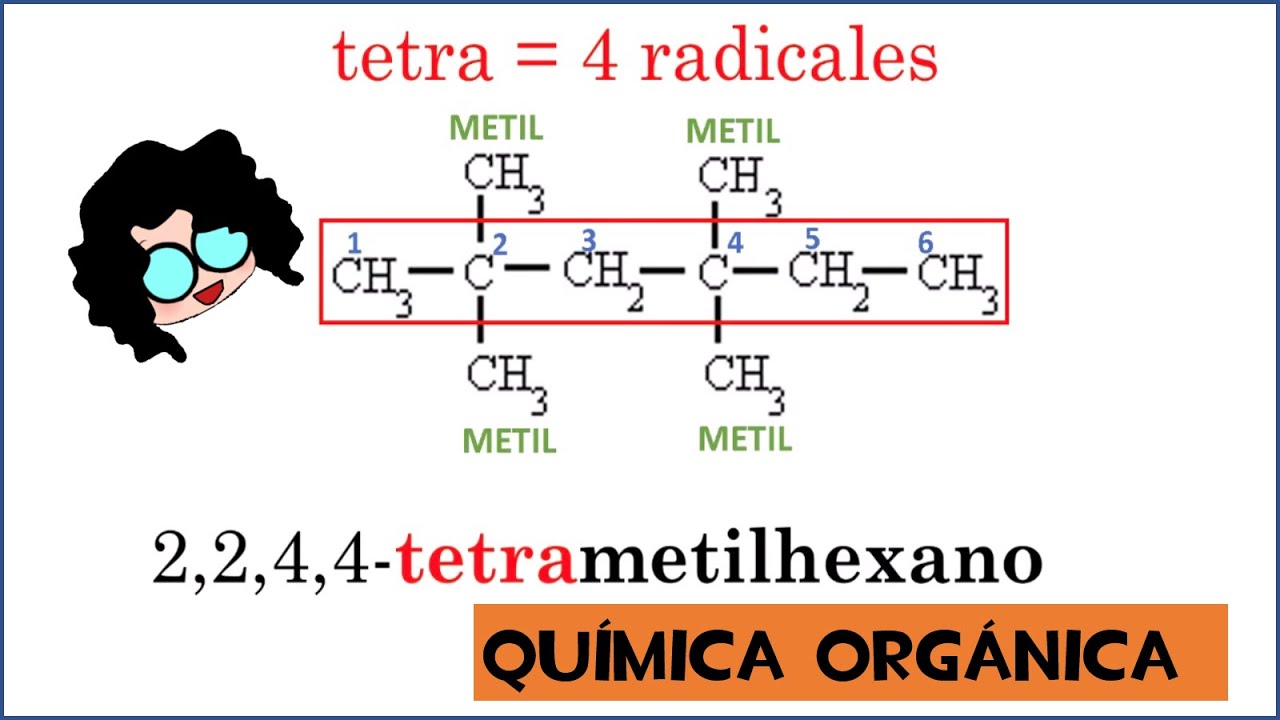
Como el átomo de carbono requiere de cuatro uniones a otros átomos, es posible que algunos compuestos se formen con uniones en las que dos átomos de carbono estan unidos al mismo átomo.
De esta forma nos referimos a átomos de carbono primarios(1°), secundarios (2 °), terciarios(3°) or cuaternarios (4 °) de acuerdo a el número de átomos de carbono unidos directamente a el, más aún esta designación se puede extender a átomos que no son de carbono o grupos unidos a carbono.Así un carbono 3 ° tiene otros tres carbonos unidos a el, y, para un alcano, un hidrógeno que por extensión se denomina hidrógeno 3 °



 las velocidades y {\displaystyle M}
las velocidades y {\displaystyle M} las masas molares.
las masas molares.